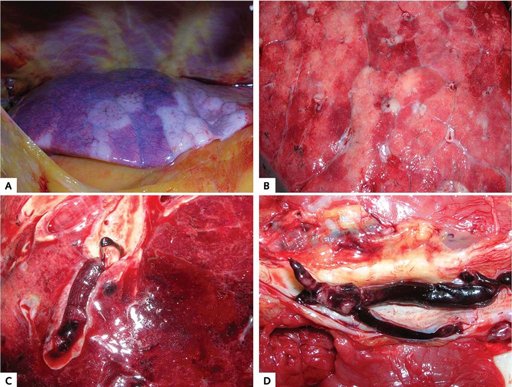
Figure 2. Résultats de l’autopsie macroscopique.
A. Aspect irrégulier de la surface pulmonaire (cas 1). B. Surface de coupe du poumon dans le cas 4. C. Embolie pulmonaire (cas 3). D. Thrombose veineuse profonde (cas 5).
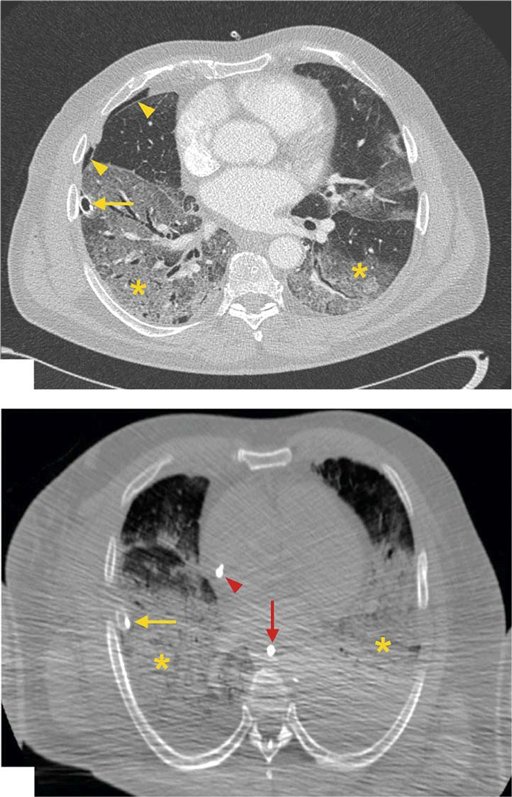
Figure 1. Imagerie par tomodensitométrie (TDM) antemortem versus post-mortem (cas 3).
Haut. La tomodensitométrie améliorée au moyen de contraste démontre les résultats antémortem: opacités bilatérales en verre dépoli dans les lobes inférieurs des deux poumons ( astérisques jaunes ) et un drain thoracique ( flèche jaune ), qui a été introduit pour traiter un pneumothorax ( pointes de flèches jaunes ). Bas. La tomodensitométrie sans amélioration du produit de contraste démontre les résultats post-mortem correspondants. Pour des raisons techniques, l’image post-mortem a une résolution inférieure. Pour protéger le personnel contre une infection potentielle, les corps ont été scannés dans un sac mortuaire à double épaisseur avec les bras positionnés le long du corps. Bien que les résultats correspondent aux images antemortem, les opacités du verre dépoli dans les deux lobes inférieurs ( astérisques jaunes) et un drain thoracique ( flèche jaune ) sont visibles. De plus, une ligne veineuse centrale ( pointe de flèche rouge ) et une sonde gastrique ( flèche rouge ) sont visibles.
Abstrait
Contexte:
Le nouveau coronavirus, le coronavirus 2 du syndrome respiratoire aigu sévère (SRAS-CoV-2), a causé plus de 210000 décès dans le monde. Cependant, on en sait peu sur les causes de décès et les caractéristiques pathologiques du virus.
Objectif:
Valider et comparer les résultats cliniques avec les données d’autopsie médicale, d’autopsie virtuelle et de tests virologiques.
Conception:
Étude prospective de cohorte.
Réglage:
Autopsies effectuées dans un seul centre médical universitaire, comme mandaté par l’État fédéral allemand de Hambourg pour les patients décédés avec une réaction en chaîne par polymérase – diagnostic confirmé de COVID-19.
Les patients:
Les 12 premiers décès consécutifs positifs au COVID-19.
Des mesures:
Une autopsie complète, comprenant une tomodensitométrie post-mortem et une analyse histopathologique et virologique, a été réalisée. Les données cliniques et l’évolution médicale ont été évaluées.
Résultats:
L’âge médian des patients était de 73 ans (intervalle de 52 à 87 ans), 75% des patients étaient de sexe masculin et le décès est survenu à l’hôpital ( n = 10) ou en ambulatoire ( n = 2). Les maladies coronariennes et l’asthme ou la bronchopneumopathie chronique obstructive étaient les comorbidités les plus courantes (50% et 25%, respectivement). L’autopsie a révélé une thrombose veineuse profonde chez 7 des 12 patients (58%) chez lesquels une thromboembolie veineuse n’était pas suspectée avant le décès; l’embolie pulmonaire était la cause directe de décès chez 4 patients. La tomodensitométrie post-mortem a révélé une infiltration réticulaire des poumons avec une consolidation bilatérale et dense sévère, alors que des lésions alvéolaires histomorphologiquement diffuses ont été observées chez 8 patients. Chez tous les patients, l’ARN du SRAS-CoV-2 a été détecté dans les poumons à des concentrations élevées; virémie chez 6 patients sur 10 et 5 patients sur 12 a montré des titres élevés d’ARN viral dans le foie, les reins ou le cœur.
Limitation:
Échantillon limité.
Conclusion:
L’incidence élevée d’événements thromboemboliques suggère un rôle important de la coagulopathie induite par le COVID-19. D’autres études sont nécessaires pour étudier le mécanisme moléculaire et l’incidence clinique globale des décès liés au COVID-19, ainsi que les interventions thérapeutiques possibles pour le réduire.
Source de financement principale:
Centre médical universitaire de Hambourg-Eppendorf.
Depuis sa première détection en décembre 2019, le nouveau coronavirus 2 du syndrome respiratoire aigu sévère (SRAS-CoV-2) s’est propagé de la province chinoise centrale du Hubei à presque tous les pays du monde ( 1 , 2 ). La plupart des personnes atteintes de COVID-19 ont une évolution bénigne de la maladie, mais environ 20% développent une évolution plus sévère avec un taux de mortalité élevé ( 3 ). Au 26 avril 2020, plus de 2,9 millions de personnes avaient reçu un diagnostic de COVID-19 et 210000 d’entre elles étaient décédées ( 4). Pourquoi le nouveau coronavirus semble avoir un taux de mortalité beaucoup plus élevé que la grippe saisonnière n’est pas complètement compris. Certains auteurs ont signalé des facteurs de risque potentiels pour une évolution plus grave de la maladie, notamment des niveaux élevés de D-dimères, un score élevé d’évaluation séquentielle des défaillances organiques et un âge plus avancé ( 5 , 6). En raison de la nouveauté de l’agent pathogène, on sait peu de choses sur les causes de décès chez les patients atteints et ses caractéristiques pathologiques spécifiques. Malgré les tests de diagnostic modernes, l’autopsie est toujours d’une grande importance et peut être une clé pour comprendre les caractéristiques biologiques du SRAS-CoV-2 et la pathogenèse de la maladie. Idéalement, les connaissances acquises de cette manière peuvent influencer les stratégies thérapeutiques et finalement réduire la mortalité. À notre connaissance, seuls 3 rapports de cas ont été publiés sur des patients COVID-19 ayant subi une autopsie complète ( 7 , 8 ). Par conséquent, dans cette étude, nous avons étudié la valeur de l’autopsie pour déterminer la cause du décès et décrire les caractéristiques pathologiques chez les patients décédés du COVID-19.
Méthodes
Étudier le design
En réponse à la propagation pandémique du SRAS-CoV-2, les autorités de l’État fédéral allemand de Hambourg ont ordonné des autopsies obligatoires chez tous les patients décédés avec un diagnostic de COVID-19 confirmé par réaction en chaîne par polymérase (PCR). La base juridique à cet égard était l’article 25 (4) de la loi allemande sur la protection contre les infections. En raison des réglementations légales, aucun décès COVID-19 n’a été exempté de cette ordonnance, même si sa cause clinique semblait évidente. La série de cas présentée ici comprend 12 autopsies consécutives, en commençant par le premier décès positif connu pour le SRAS-CoV-2 survenu à Hambourg (la deuxième plus grande ville d’Allemagne, avec 1,8 million d’habitants). Toutes les autopsies ont été réalisées au département de médecine légale du centre médical universitaire de Hambourg-Eppendorf. Le comité d’éthique de la Chambre des médecins de Hambourg a été informé de l’étude (no. WF-051/20). L’étude a été approuvée par le comité d’examen clinique institutionnel local et s’est conformée à la déclaration d’Helsinki. Chez tous les patients décédés, une tomodensitométrie post-mortem (PTME) et une autopsie complète, y compris une évaluation histopathologique et virologique, ont été réalisées. Les dossiers cliniques ont été vérifiés pour les conditions médicales préexistantes et les médicaments, l’évolution médicale actuelle et les résultats de diagnostic antemortem.
PTME, autopsie et examen histologique
Un examen tomodensitométrique a été effectué au Département de médecine légale avec un scanner multidétecteur Philips Brilliance à 16 coupes conformément à un protocole établi ( 9). En bref, une tomodensitométrie du corps entier a été réalisée du haut à la cuisse (épaisseur de coupe, 1 mm; pas, 1,5; 120 kV; 230 à 250 mAs), complétée par des scans dédiés du thorax avec une résolution plus élevée (épaisseur de coupe, 0,8 mm ; pas, 1,0; 120 kV; 230 à 250 mAs). Nous avons effectué des examens externes et des autopsies du corps entier sur toutes les personnes décédées avec une positivité au SRAS-CoV-2 (PCR confirmée) dès que possible après avoir pris les précautions de sécurité appropriées (en utilisant un équipement de protection individuelle avec un enfilage et un retrait appropriés), en suivant les directives de l’allemand Association of Pathologists, qui sont étroitement alignées sur les directives internationales pertinentes. Les recommandations récemment publiées pour la réalisation d’autopsies en cas de suspicion de COVID-19 ont été prises en compte ( 10). L’intervalle entre le décès et l’imagerie post-mortem et l’autopsie (intervalle post-mortem) variait de 1 à 5 jours. Au cours de l’autopsie, des échantillons de tissus pour l’histologie ont été prélevés sur les organes suivants: cœur, poumons, foie, reins, rate, pancréas, cerveau, prostate et testicules (chez les hommes), ovaires (chez les femmes), intestin grêle, veine saphène, carotide commune artère, pharynx et muscle.
Pour les tests virologiques, nous avons prélevé de petits échantillons de cœur, de poumons, de foie, de rein, de veine saphène et de pharynx et avons échantillonné le sang veineux.
Les échantillons de tissus pour l’examen histopathologique ont été fixés dans du formaldéhyde tamponné à 4% et traités selon une procédure standard sur des lames colorées à l’hématoxyline-éosine. Pour les échantillons pulmonaires, nous avons également utilisé le marqueur de kératine AE1 / AE3 (Dako) pour l’immunohistochimie.
PCR quantitative de transcription inverse ARN SARS-CoV-2 à partir de tissu
Les échantillons de tissus ont été broyés en utilisant des billes de céramique (kit de lyse Precellys) et extraits en utilisant une extraction automatisée d’acide nucléique (MagNA Pure 96 [Roche]) selon les recommandations du fabricant. Pour la quantification des virus dans les tissus, un test précédemment publié a été adopté avec des modifications ( 11 ). Une PCR en temps réel en une étape a été effectuée sur le système LightCycler 480 (Roche) en utilisant un kit de contrôle d’ARN en une étape (Roche) comme mélange principal. La valeur C t (seuil de cycle) pour l’ARN cible du SARS-CoV-2 (fluorescéine) et le contrôle de l’ARN du processus entier (Cy5) a été déterminée en utilisant la deuxième méthode du maximum dérivé. Pour la quantification, l’ARN standard transcrit in vitro du gène E du SRAS-CoV-2 a été utilisé ( 12). Ces échantillons ont également été analysés dans une étude portant sur le tropisme rénal du SRAS-CoV-2 (Puelles V, et al. Tropisme multi-organes et rénal du SRAS-CoV-2. En préparation).
Analyses statistiques
Les données qui étaient normalement distribuées sont présentées comme des moyennes (SD); les données en dehors de la distribution normale sont présentées sous forme de médianes (plages). Les variables catégorielles ont été résumées sous forme de nombres et de pourcentages. Toutes les données ont été analysées avec Statistica, version 13 (StatSoft).
Rôle de la source de financement
Le promoteur n’a pas été impliqué dans la conception ou la conduite de l’étude, ni dans l’analyse des données ou dans la décision de soumettre le manuscrit.
Résultats
Donnée clinique
L’âge médian des 12 patients inclus dans cette étude était de 73 ans (intervalle interquartile, 18,5 ans); 25% étaient des femmes. Pour tous les patients, des conditions médicales chroniques préexistantes, telles que l’obésité, les maladies coronariennes, l’asthme ou la maladie pulmonaire obstructive chronique, la maladie artérielle périphérique, le diabète sucré de type 2 et les maladies neurodégénératives, pourraient être identifiées ( tableau 1). Deux patients sont décédés de l’hôpital après une réanimation cardio-pulmonaire infructueuse, 5 sont décédés après un traitement dans l’unité de soins intensifs et les 5 autres avaient une directive avancée pour les meilleurs soins de soutien et sont décédés dans le service de soins non intensifs. Les résultats de laboratoire pour la chimie clinique, l’hématologie et la coagulation n’étaient pas disponibles pour les patients décédés hors de l’hôpital. Chez les patients restants, les caractéristiques les plus frappantes du test de laboratoire initial étaient des taux élevés de lactate déshydrogénase (médiane, 7,83 µkat / L [intervalle, 2,71 à 11,42 µkat / L]), D-dimère (disponible pour 5 patients; médiane, 495,24 nmol / L [intervalle, 20,38 à> 1904,76 nmol / L]) et protéine C-réactive (médiane, 189 mg / L [intervalle, 18 à 348 mg / L]), ainsi qu’une thrombopénie légère dans 4 cas sur 10 les patients.Le tableau 2 donne un aperçu des premiers résultats de laboratoire.
Autopsie
Dans 4 cas (1, 3, 4 et 12), une embolie pulmonaire massive était à l’origine du décès, les thrombus provenant des veines profondes des membres inférieurs. Dans 3 autres cas (5, 8 et 11), une thrombose veineuse profonde fraîche était présente en l’absence d’embolie pulmonaire. Dans tous les cas de thrombose veineuse profonde, les deux jambes étaient impliquées ( Figure 2 ). Chez 6 des 9 hommes (deux tiers) inclus dans l’étude, une thrombose fraîche était également présente dans le plexus veineux prostatique ( figure 1 en annexe ).
Dans les 12 cas, la cause du décès a été trouvée dans les poumons ou dans le système vasculaire pulmonaire. Cependant, la différenciation macroscopique de la pneumonie virale avec des lésions alvéolaires diffuses subséquentes (un diagnostic histologique) de la pneumonie bactérienne n’était pas toujours possible. Typiquement, les poumons étaient encombrés et lourds, avec un poids pulmonaire combiné maximal de 3420 g dans le cas 11. Le poids moyen combiné des poumons était de 1988 g (médiane, 2088 g). Le poids standard des poumons pour les hommes et les femmes est de 840 g et 639 g, respectivement ( 13 , 14 ). Seuls les cas 6 et 9 présentaient un poids pulmonaire relativement faible: 550 g et 890 g, respectivement ( tableau annexe 1). La surface du poumon présentait souvent une pleurésie légère et un motif irrégulier distinct, avec des zones pâles alternant avec des zones hypercapillarisées bleu rougeâtre légèrement saillantes et fermes. Sur les surfaces de coupe, ce motif était également visible ( figure 2 ). La consistance du tissu pulmonaire était ferme mais friable. Dans 8 cas, toutes les parties des poumons ont été affectées par ces changements. Les cas 6, 7 et 9 – survenant chez les 3 femmes de la série de cas – présentaient des changements compatibles avec une bronchopneumonie focale purulente. Macroscopiquement, aucun changement n’a été observé en dehors des poumons et des voies respiratoires, à l’exception d’une splénomégalie dans 3 cas, ce qui suggérait une infection virale.
Au cours de l’autopsie, tous les cas, à l’exception du cas 6, présentaient une maladie cardiaque préexistante, y compris une sclérose coronarienne de haut grade (7 sur 12); cicatrisation myocardique, indiquant une cardiopathie ischémique (6 sur 12); et cardiomyopathie congestive. Le poids moyen du cœur était de 503 g (médiane, 513 g). En plus de cette constatation, les maladies d’accompagnement les plus courantes étaient l’emphysème pulmonaire (6 sur 12) et l’entérite ischémique (3 sur 12). Ces conditions étaient souvent connues du médecin traitant avant le décès (comparer les colonnes 4 et 10 du tableau 1 ). Les résultats de l’autopsie macroscopique sont présentés organe par organe dans le tableau 2 de l’annexe et les résultats pulmonaires dans le tableau 1 .
Une nette tendance à l’obésité a été observée parmi les cas (indice de masse corporelle moyen, 28,7 kg / m 2 ; médiane, 28,7 kg / m 2 ). Cependant, le cas 9, impliquant un patient avec une tumeur neuroendocrine connue du poumon, a présenté une cachexie sévère (indice de masse corporelle, 15,4 kg / m 2 ). Les conditions comorbides trouvées sont résumées dans le tableau 1 .
Histologie
L’histopathologie des poumons a montré des lésions alvéolaires diffuses, compatibles avec un syndrome de détresse respiratoire aiguë précoce dans 8 cas. Les résultats prédominants étaient les membranes hyalines ( figures 3 , A et B ), les pneumocytes activés, les thromboemboles microvasculaires, la congestion capillaire et l’œdème interstitiel enrichi en protéines. Comme décrit par Wang et ses collègues ( 15 ), un degré modéré d’infiltrats inflammatoires concordait avec la leucopénie cliniquement décrite chez les patients atteints de COVID-19 et une infiltration prédominante de lymphocytes correspondait au tableau d’une pathogenèse virale. Dans les stades ultérieurs, la métaplasie squameuse était présente ( Figure 3 , C). Les changements à long terme, tels que la destruction des cloisons alvéolaires et l’infiltration lymphocytaire des bronches, étaient souvent visibles comme des conditions préexistantes. Quatre cas (6, 8, 9 et 10) n’ont montré aucun dommage alvéolaire diffus mais une infiltration granulocytaire étendue des alvéoles et des bronches, ressemblant à une bronchopneumonie bactérienne focale. Histologiquement, les thromboemboles étaient détectables dans les cas 1, 3, 4 et 5 ( Figure 3 , D ). Des microthrombi ont été régulièrement trouvés dans les petites artères pulmonaires, parfois dans la prostate, mais pas dans d’autres organes.
En plus des changements pulmonaires décrits dans le tableau 1 , il y avait des résultats histologiques isolés qui pourraient indiquer une infection virale. La muqueuse pharyngée a été examinée dans 7 cas. Chez 6 d’entre eux, une hyperémie et une alternance d’infiltrats denses, principalement lymphocytaires, ont été retrouvées comme signes de pharyngite chronique. Dans 1 cas (cas 3), une myocardite lymphocytaire a été observée dans le ventricule droit ( figure 2 en annexe ). Les modifications histologiques restantes étaient compatibles avec des modifications de choc chez une partie du patient décédé (foie, reins, intestin) ou correspondaient à la pathologie préexistante indépendante du virus déterminée macroscopiquement (telle que la cardiomyopathie ischémique).
Outre les résultats liés à l’infection par le SRAS-CoV-2, les patients ont présenté d’autres résultats histopathologiques liés à leurs affections chroniques préexistantes, notamment l’hypertrophie des fibres myocardiques ou la cicatrisation du myocarde. Les veines périphériques, y compris celles obstruées par des thrombus, n’ont montré aucune anomalie sur la coloration à l’hématoxyline-éosine.
Résultats PCR
La PCR quantitative de transcription inverse a détecté l’ARN du SRAS-CoV-2 dans les poumons des 12 patients (plage de 1,2 × 10 4 à 9 × 10 9 copies / ml) et dans le pharynx de 9 patients. Six patients ont présenté une virémie modérée (<4 × 10 4 copies / ml). Chez 5 de ces patients, de l’ARN viral a également été détecté dans d’autres tissus (cœur, foie ou rein) à des concentrations dépassant la virémie. Les patients sans virémie présentaient une charge virale nulle ou faible dans les autres tissus. Seuls 4 patients avaient un ARN viral détectable dans le cerveau et la veine saphène.
Discussion
Dans cette étude d’autopsie de 12 patients consécutifs décédés du COVID-19, nous avons trouvé une incidence élevée de thrombose veineuse profonde (58%). Un tiers des patients avaient une embolie pulmonaire comme cause directe de décès. De plus, des lésions alvéolaires diffuses ont été mises en évidence par histologie chez 8 patients (67%).
À notre connaissance, il s’agit de la première série de cas résumant et comparant les données cliniques de cas consécutifs de COVID-19 avec les résultats obtenus par une autopsie complète, complétée par la PTME, l’histologie et la virologie.
Le taux élevé d’embolie pulmonaire mortelle à l’autopsie est bien corrélé à l’échec de la réanimation de 3 patients sur 4, dont 2 sont décédés hors de l’hôpital. En dehors de cela, aucune preuve préclinique d’embolie pulmonaire ou de thrombose veineuse profonde n’a été rapportée.
Dans les études qui ont examiné des patients décédés atteints de COVID-19 sans se fier à l’autopsie, aucune augmentation des taux d’embolie pulmonaire n’a été observée cliniquement. Cependant, on sait que de nombreux cas d’embolie pulmonaire restent cliniquement négligés et sont souvent associés à une mort soudaine et inattendue. Cela peut avoir été aggravé par la méthode de diagnostic du COVID-19 en Allemagne, qui est basée sur des tests PCR plutôt que sur une imagerie tomographique calculée en raison de préoccupations concernant l’infection du personnel médical et d’autres patients. Un rapport récent décrit les caractéristiques cliniques de 85 cas mortels de COVID-19 à Wuhan ( 16 ). Outre l’insuffisance respiratoire, la cause du décès était une défaillance multiorganique dans 16% des cas et un arrêt cardiaque dans 9%. Aucune autopsie n’a été réalisée. L’étalon-or pour identifier la cause du décès est toujours l’autopsie (17 ). Cependant, les taux d’autopsie à l’hôpital ont diminué dans le monde entier au cours des dernières décennies. De plus, en raison du risque potentiel des pathologistes d’infection par le SRAS-CoV-2, très peu d’autopsies ont été pratiquées dans le monde ( 18 ). À notre connaissance, seuls 3 rapports de cas ont été publiés sur des patients atteints de COVID-19 ayant subi une autopsie complète et quelques autres dans lesquels seul le tissu pulmonaire a été examiné ( 7 , 8 ).
D’autres chercheurs ont décrit la coagulopathie comme une complication fréquente chez les patients atteints de COVID-19 sévère ( 5 , 6 , 19 ). Dans une étude récente de 191 patients atteints de COVID-19, 50% de ceux décédés avaient une coagulopathie, contre 7% des survivants. Des niveaux de D-dimères supérieurs à 1 000 µg / L étaient associés à une issue fatale ( 6 ).
Le COVID-19 peut prédisposer à la thromboembolie veineuse de plusieurs manières. Le système de coagulation peut être activé par de nombreux virus différents, y compris le VIH, le virus de la dengue et le virus Ebola ( 20 , 21 ). En particulier, les infections à coronavirus peuvent être un déclencheur de thromboembolie veineuse, et plusieurs mécanismes pathogéniques sont impliqués, y compris un dysfonctionnement endothélial, caractérisé par des niveaux accrus de facteur von Willebrand; inflammation systémique, par activation du récepteur de type Toll; et un état procoagulateur, par l’activation de la voie du facteur tissulaire ( 22 ). Dans un sous-groupe de patients atteints de COVID-19 sévère, des taux plasmatiques élevés de cytokines pro-inflammatoires ont été observés ( 23). L’activation directe de la cascade de coagulation par une tempête de cytokines est envisageable. Avec COVID-19, une hypoxémie sévère se développe chez certains patients ( 24 ). La formation de thrombus dans des conditions hypoxiques est facilitée à la fois dans les modèles animaux de thrombose et chez l’homme. La réponse vasculaire à l’hypoxie est principalement contrôlée par les facteurs de transcription inductibles par l’hypoxie, dont les gènes cibles comprennent plusieurs facteurs qui régulent la formation de thrombus ( 25 ). Enfin, des causes indirectes, telles que les dommages à médiation immunitaire par les anticorps antiphospholipides, peuvent partiellement y contribuer, comme l’ont supposé Zhang et ses collègues ( 26 ).
Les résultats macroscopiques de notre série d’autopsies – avec des poumons plutôt lourds, consolidés, friables, essentiellement sans air dans la plupart des cas – étaient impressionnants et expliquent les difficultés à ventiler suffisamment certains de ces patients. Les changements histopathologiques dans la plupart de nos cas avec des lésions alvéolaires diffuses comme résultat principal ressemblent à ceux décrits par Xu et ses collègues ( 7 ) et Barton et ses collègues ( 8 ), qui ont rapporté des cas uniques; Zhang et ses collègues ( 26 ), qui ont rapporté une biopsie pulmonaire chez un patient avec une positivité au SRAS-CoV-2; et Tian et ses collègues ( 27), qui a décrit des résultats pulmonaires macroscopiques et histologiques chez 2 patients atteints d’un cancer du poumon qui ont reçu des résultats positifs au test SARS-CoV-2. Cependant, le tableau complet des lésions alvéolaires diffuses semble être plus répandu chez les patients plus jeunes avec moins de maladies préexistantes et une survie plus longue, tandis que les patients plus âgés avec des conditions plus comorbides ont tendance à mourir dans les premiers stades de la maladie.
Conformément aux résultats cliniques, macroscopiques et histopathologiques, la PCR a détecté la concentration la plus élevée d’ARN du SRAS-CoV-2 dans les tissus pulmonaires et pharyngés. Il est intéressant de noter que chez la plupart des patients atteints de maladie, des titres élevés d’ARN ont également été détectés dans des échantillons post-mortem. La pertinence clinique de ceci n’est pas encore claire. La clairance de l’ARN viral du sang 7 jours après la transfusion de plasma convalescent COVID-19 a été associée à une amélioration clinique substantielle, mais les études n’ont pas montré de corrélation entre la virémie et le syndrome de détresse respiratoire aiguë chez les patients atteints de COVID-19 sévère ( 28 , 29 ). Comme chez les patients atteints du SRAS-CoV-1, chez lesquels une réplication virale pourrait être détectée dans d’autres organes, notamment le foie, les reins, la rate et le cerveau ( 30), nous avons détecté de l’ARN viral à des titres élevés dans d’autres organes (foie, rein et cœur) chez 5 patients. Ces données suggèrent que le SRAS-CoV-2 peut se propager via la circulation sanguine et infecter d’autres organes. Pour le prouver, les intermédiaires de réplication doivent être détectés.
L’étude actuelle avait certaines limites. Premièrement, la taille de l’échantillon était petite, conduisant peut-être à une surestimation du taux d’embolie pulmonaire. Cependant, les observations cliniques et post-mortem concordent bien avec les connaissances actuelles sur la pathologie du SRAS-CoV-2. Cela inclut la distribution par sexe et par âge ainsi que les conditions préexistantes chez les patients, mais aussi les résultats histologiques. Deuxièmement, bien que les titres viraux dans les écouvillons (pharynx) pris longitudinalement jusqu’à 7 jours après la mort soient restés similaires, nous manquons de données sur la façon dont les processus post-mortem affectent les titres et la dynamique viraux dans différents tissus et liquides corporels. De plus, le test PCR quantitatif utilisé ne peut pas faire la distinction entre l’ARN génomique et sous-génomique. Comme indiqué précédemment, pour prouver la réplication virale, la détection d’intermédiaires de réplication ou d’ARN antigénomique serait nécessaire.
En conclusion, nous avons trouvé une incidence élevée d’événements thromboemboliques chez les patients atteints de COVID-19. Lorsqu’une détérioration hémodynamique survient chez un patient atteint de COVID-19, une embolie pulmonaire doit toujours être suspectée. Il semble plausible que les patients atteints de COVID-19 dont les taux de D-dimères augmentent, signe de coagulopathie, puissent bénéficier d’un traitement anticoagulant ( 31 ). Comme démontré dans notre cohorte, cela pourrait être important pour les patients hospitalisés et les patients ambulatoires. Dans ce contexte, certaines sociétés professionnelles ont déjà fait des recommandations pour un traitement antithrombotique pour les patients atteints de COVID-19 ( 32 ). Cependant, les preuves solides restent rares et d’autres études prospectives sont nécessaires de toute urgence pour confirmer et valider ces résultats.
Cet article a été publié sur Annals.org le 6 mai 2020.
* Drs. Wichmann et Sperhake partagent la première paternité.
† Drs. Püschel et Kluge partagent la dernière paternité.




