
la thrombose veineuse profonde, l’embolie pulmonaire et l’hémorragie
L’infection est-elle plus à risque que la vaccination ?
Ces risques de thrombose sont également connus pour la vaccination contre le virus. Dans une étude britannique, publiée en août 2021 dans le British Medical Journal, des chercheurs affirment qu’il existe un « risque accru » de développer cet effet secondaire après avoir reçu une injection de vaccin anti-Covid, mais que ce risque était près de 200 fois « plus faible que celui associé à l’infection par le SRAS-CoV-2 ».
Dans une étude publiée cette semaine, des chercheurs suédois ont étudié le risque de développer une thrombose veineuse profonde ou une embolie pulmonaire après une contamination au virus. Ce risque est présent jusqu’à 6 mois après une infection.
Une infection au SARS-CoV-2 est susceptible d’avoir de lourdes conséquences sur le long terme, pour la santé d’une personne contaminée. Selon une étude publiée mercredi 6 avril dans le British medical Journal (BMJ), le Covid-19 accroît le risque de développer des caillots sanguins graves jusqu’à six mois après l’infection.
Que dit cette nouvelle étude ?
Il était déjà connu que le Covid-19 augmentait le risque de caillots sanguins graves (connus sous le nom de thrombose veineuse), mais on avait moins d’informations sur la durée pendant laquelle ce risque était accru et s’il a varié pendant les différentes vagues épidémiques.
Cette étude suédoise apporte des données nouvelles à ce sujet. Elle révèle un risque accru de thrombose veineuse profonde (un caillot sanguin dans la jambe) jusqu’à trois mois après l’infection au Covid-19, d’embolie pulmonaire (un caillot de sang dans les poumons) jusqu’à six mois après et d’un événement hémorragique jusqu’à deux mois après.
Quelles personnes sont les plus à risques ?
Ce risque est plus élevé chez les patients atteints de comorbidités et ceux atteints d’un Covid-19 sévère. Il était plus marqué pendant la première vague pandémique par rapport aux deuxième et troisième vagues, souligne aussi l’étude. Selon les chercheurs, les risques accrus observés pendant la première vague par rapport aux deux suivantes pourraient s’expliquer par les améliorations ultérieures des traitements et de la couverture vaccinale chez les patients plus âgés.
L’infection est-elle plus à risque que la vaccination ?
Ces risques de thrombose sont également connus pour la vaccination contre le virus. Dans une étude britannique, publiée en août 2021 dans le British Medical Journal, des chercheurs affirment qu’il existe un « risque accru » de développer cet effet secondaire après avoir reçu une injection de vaccin anti-Covid, mais que ce risque était près de 200 fois « plus faible que celui associé à l’infection par le SRAS-CoV-2 ».
Au total, 1 057 174 personnes atteintes de covid-19 (517 434 (49 %) hommes, 539 740 (51 %) femmes) ont été signalées à SmiNet ( tableau 1 ). L’âge moyen était de 40,2 (ET 19) ans. L’ensemble de données comprenait 42 réinfections potentielles ; cinq d’entre eux portaient exactement la même date, bien qu’à un an d’intervalle, ce qui indique une erreur de codage. Au total, 4 076 342 participants témoins appariés ont été identifiés.
La source de données
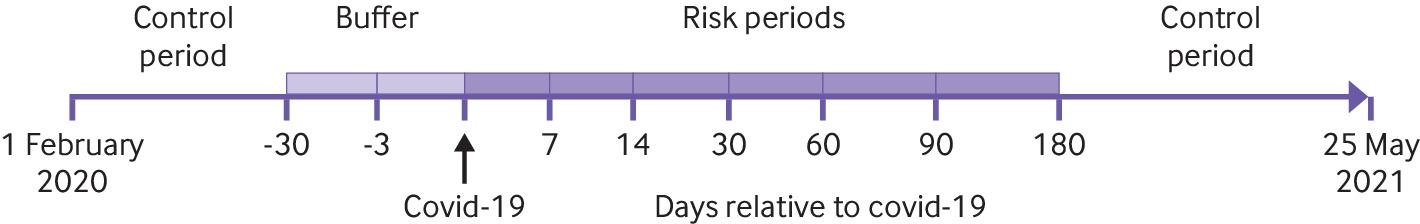
Les numéros d’identification personnels des personnes testées positives pour le SRAS-CoV-2 entre le 1er février 2020 et le 25 mai 2021 ont été envoyés par le système de surveillance des maladies transmissibles, SmiNet (Agence de santé publique de Suède), à Statistics Sweden. Nous avons défini la date covid-19 comme la plus ancienne à partir de la date d’apparition de la maladie, de la date de l’échantillon, de la date du diagnostic ou de la date de notification à SmiNet (voir tableau supplémentaire 1). Seules les premières infections ont été incluses. Statistics Sweden a identifié quatre personnes testées négatives (témoins) pour chaque participant testé positif pour le SRAS-CoV-2, appariées sur l’âge, le sexe et le comté de résidence. La date index pour les participants témoins était la date correspondante pour les participants testés positifs pour le SRAS-CoV-2. Les numéros d’identification personnels des personnes testées positives ou négatives pour le SRAS-CoV-2 ont été croisés avec le registre des patients hospitalisés (cas covid-19 : 1987-2021, témoins : 1997-2021), le registre des patients externes (1997-2021), Cause des décès (2020-21), le registre des soins intensifs (2020-21), le registre des médicaments prescrits du Conseil national suédois de la santé et du bien-être et le registre suédois des soins intensifs. Nous avons calculé l’indice de comorbidité de Charlson pondéré pour chaque participant.6 7
La taille de l’échantillon nécessaire pour identifier un effet aigu cliniquement pertinent (taux d’incidence ou risque relatif de 2) avec une puissance de 90 % au cours d’une période de risque de 30 jours était de 181 événements dans l’étude de séries de cas auto-contrôlées et de 112 événements dans la cohorte appariée. étude. La taille de l’échantillon nécessaire pour identifier un effet cliniquement significatif (taux d’incidence ou risque relatif de 1,5) avec une puissance de 90 % sur la période de risque globale de 180 jours était de 258 événements dans l’étude de séries de cas auto-contrôlées et de 354 événements dans l’étude de cohorte appariée. . Les calculs de taille d’échantillon ont été effectués a priori.
Aucune donnée ne manquait dans notre analyse.
Participation des patients et du public
L’accès aux données historiques pseudonymisées de nos registres nationaux suédois est limité par la loi et n’est pas accessible au public. Notre question de recherche devait être claire et ciblée pour nous permettre de demander les données. Comme notre étude était liée à la recherche sur le covid-19, il y avait une urgence pour l’analyse. De plus, la courbe d’apprentissage pour extraire et analyser les données était abrupte. Cette étude a été conçue dans une perspective interne, et nous n’avons pas été financés pour la participation des patients ou du public, et nous n’avions pas non plus envisagé la possibilité d’impliquer les patients ou le public d’autres manières telles que l’examen du manuscrit ou la diffusion des résultats. Nous apprécions le rôle des patients en tant que partenaires dans la recherche et sommes impatients de publier de futures recherches qui incluent des patients et des membres du public.
Résultats
Au total, 1 057 174 personnes atteintes de covid-19 (517 434 (49 %) hommes, 539 740 (51 %) femmes) ont été signalées à SmiNet ( tableau 1 ). L’âge moyen était de 40,2 (ET 19) ans. L’ensemble de données comprenait 42 réinfections potentielles ; cinq d’entre eux portaient exactement la même date, bien qu’à un an d’intervalle, ce qui indique une erreur de codage. Au total, 4 076 342 participants témoins appariés ont été identifiés.
Conclusions et implications politiques
Les résultats actuels ont des implications politiques majeures. Nos résultats soutiennent sans doute la thromboprophylaxie pour éviter les événements thrombotiques, en particulier pour les patients à haut risque, 23 et renforcent l’importance de la vaccination contre le covid-19. Il reste à établir si l’infection par le SRAS-CoV-2 augmente le risque de thromboembolie veineuse ou de saignement plus que pour les infections respiratoires, comme la grippe, mais aussi si la période de thromboprophylaxie après le covid-19 doit être prolongée. De futures recherches cliniques seraient bénéfiques dans ce contexte.
Qu’est-ce qu’on sait déjà à ce sujet
-
Il est bien connu que le covid-19 augmente le risque de thromboembolie veineuse
-
Il existe moins de preuves sur la durée pendant laquelle ce risque est accru, si le risque a changé pendant les vagues pandémiques et si le covid-19 augmente également le risque de saignement
Ce que cette étude ajoute
-
Les résultats de cette étude suggèrent que le covid-19 est un facteur de risque indépendant de thrombose veineuse profonde, d’embolie pulmonaire et de saignement, et que le risque de ces résultats est augmenté pendant trois, six et deux mois après le covid-19, respectivement.
-
Cette étude a également révélé un risque plus élevé d’événements chez les patients présentant des comorbidités, les patients atteints de covid-19 plus sévère et pendant la première vague pandémique par rapport aux deuxième et troisième vagues



